Protein có bao nhiêu bậc cấu trúc là một câu hỏi thú vị, không chỉ với các nhà khoa học mà còn với những ai đam mê tìm hiểu về công nghệ sinh học và dinh dưỡng. Để hiểu rõ hơn về protein, chúng ta cần đi sâu vào từng cấp độ cấu trúc của nó và vai trò quan trọng trong sự sống.
Protein có bao nhiêu bậc cấu trúc? Khái niệm và tầm quan trọng của cấu trúc bậc
Protein là một đại phân tử sinh học quan trọng, đóng vai trò thiết yếu trong mọi hoạt động sống của cơ thể. Cấu trúc của protein không chỉ đơn thuần là một chuỗi axit amin mà còn có sự sắp xếp phức tạp theo nhiều bậc khác nhau.
Khái niệm về cấu trúc bậc của protein
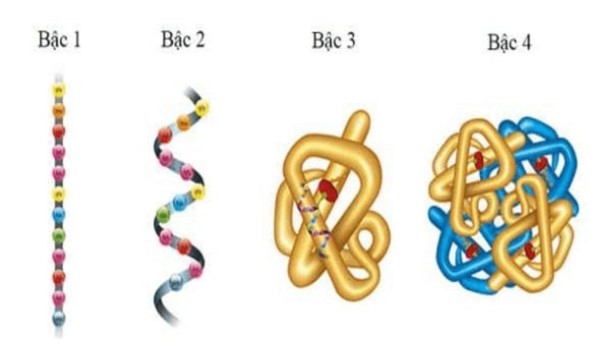
Cấu trúc bậc của protein đề cập đến cách các axit amin liên kết với nhau và sắp xếp trong không gian, tạo nên hình dạng đặc trưng của phân tử protein. Sự hình thành cấu trúc này ảnh hưởng trực tiếp đến chức năng sinh học của protein trong cơ thể.
Có bốn bậc cấu trúc chính của protein:
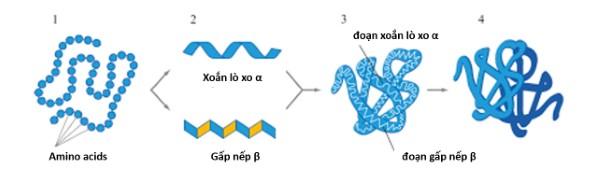
- Cấu trúc bậc một: Chuỗi axit amin liên kết với nhau bằng liên kết peptide, tạo nên trình tự đặc trưng cho mỗi loại protein.
- Cấu trúc bậc hai: Chuỗi polypeptide bắt đầu cuộn xoắn (α-helix) hoặc gấp nếp (β-sheet) nhờ vào liên kết hydro giữa các nhóm peptid.
- Cấu trúc bậc ba: Sự xoắn và gấp khúc của chuỗi polypeptide tiếp tục tạo thành hình dạng ba chiều đặc trưng, quyết định trực tiếp đến chức năng protein.
- Cấu trúc bậc bốn: Một số protein có nhiều chuỗi polypeptide liên kết với nhau để tạo thành một phức hợp chức năng hoàn chỉnh.
Tầm quan trọng của cấu trúc bậc của protein
Cấu trúc của protein đóng vai trò quan trọng trong việc duy trì và điều phối các hoạt động sinh học trong cơ thể. Một số điểm nổi bật về tầm quan trọng của cấu trúc protein gồm:
- Quyết định chức năng sinh học: Hình dạng không gian của protein ảnh hưởng đến khả năng tương tác với các phân tử khác, từ đó xác định vai trò của nó trong cơ thể.
- Liên quan đến bệnh lý: Những thay đổi bất thường trong cấu trúc protein có thể gây ra các bệnh như Alzheimer, Parkinson, hoặc các rối loạn di truyền.
- Ứng dụng trong y học và công nghệ sinh học: Việc nghiên cứu cấu trúc protein giúp phát triển thuốc điều trị bệnh, sản xuất enzyme công nghiệp và cải tiến công nghệ sinh học.
Nhìn chung, việc hiểu rõ về các bậc cấu trúc của protein không chỉ giúp chúng ta có cái nhìn sâu hơn về sự sống mà còn mở ra nhiều ứng dụng quan trọng trong khoa học và y học.
Phân tích chi tiết bốn bậc cấu trúc của protein
Khi nhắc đến protein, điều kiện tiên quyết là phải hiểu rõ bốn bậc cấu trúc của nó. Mỗi bậc cấu trúc đều có đặc điểm và vai trò riêng, tạo nên tính năng động và đa dạng của protein trong cơ thể.
Tổng quan về bốn bậc cấu trúc
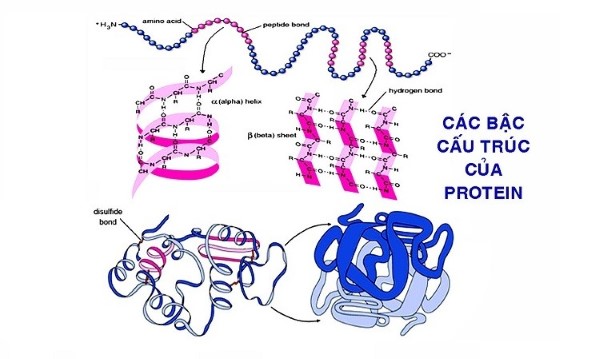
Bốn bậc cấu trúc của protein bao gồm:
- Cấu trúc bậc một: Chuỗi polypeptide đơn giản.
- Cấu trúc bậc hai: Các hình dạng nhất định như α-helix và β-sheet.
- Cấu trúc bậc ba: Gấp cuộn không gian của chuỗi polypeptide.
- Cấu trúc bậc bốn: Sự tương tác giữa các chuỗi polypeptide khác nhau.
Mỗi bậc cấu trúc phụ thuộc vào bậc trước đó và tạo thành một mạng lưới phức tạp giúp protein thực hiện chức năng của mình.
Tính chất chung của cấu trúc protein
Tất cả các bậc cấu trúc của protein đều bị ảnh hưởng bởi yếu tố môi trường như pH, nhiệt độ và nồng độ muối. Sự ổn định cấu trúc trong protein rất quan trọng vì bất kỳ thay đổi nào trong các yếu tố này cũng có thể dẫn đến sự biến tính của protein, làm giảm hoặc mất hoàn toàn chức năng của nó.
Vai trò của nghiên cứu cấu trúc protein
Nghiên cứu về cấu trúc protein đã giúp chúng ta hiểu rõ hơn về cơ chế hoạt động của các bệnh tật và tìm kiếm phương pháp điều trị hiệu quả hơn. Nhờ sự phát triển của công nghệ sinh học, chúng ta có thể xác định cấu trúc protein chính xác và từ đó áp dụng vào các ứng dụng thực tiễn.
Cấu trúc bậc một của Protein: Chuỗi polypeptide và liên kết peptide
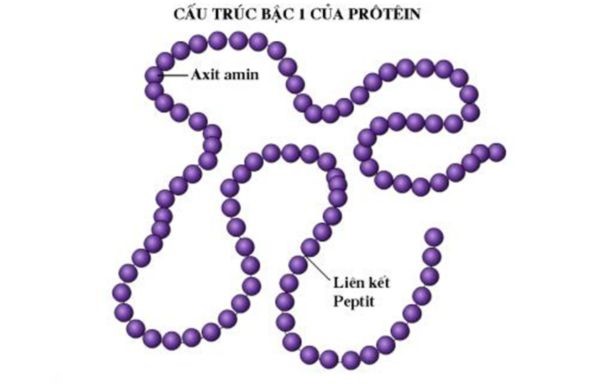
Cấu trúc bậc một của protein đề cập đến chuỗi axit amin liên kết với nhau bằng các liên kết peptide. Đây là bậc cấu trúc đơn giản nhất nhưng cũng là nền tảng cho tất cả các bậc còn lại.
Liên kết peptide
Liên kết peptide hình thành khi nhóm amino của một axit amin kết hợp với nhóm carboxyl của axit amin khác, tạo ra một liên kết hóa học với sự giải phóng nước. Quá trình này được gọi là phản ứng ngưng tụ. Những liên kết này rất mạnh mẽ và tạo nên khung xương cho chuỗi polypeptide.
Các chuỗi polypeptide có thể dài từ vài chục đến hàng ngàn axit amin. Sự sắp xếp của các axit amin này theo thứ tự cụ thể quyết định chức năng của protein.
Tính chất của chuỗi polypeptide
Chuỗi polypeptide có khả năng tạo ra nhiều cấu trúc khác nhau tùy thuộc vào thứ tự của các axit amin. Chính sự đa dạng này khiến cho mỗi loại protein đều có những đặc điểm và chức năng riêng biệt. Khi các axit amin mang điện tích khác nhau, chúng có thể tương tác với nhau và ảnh hưởng đến cấu trúc tổng thể của protein.
Ví dụ minh họa về cấu trúc bậc một
Một ví dụ điển hình cho cấu trúc bậc một là insulin, một loại hormone quan trọng trong việc điều chỉnh đường huyết. Chuỗi axit amin trong insulin được sắp xếp rất cụ thể, từ đó tạo ra một protein hoạt động hiệu quả trong việc kiểm soát mức glucose trong máu.
Cấu trúc bậc hai của Protein: α-helix, β-sheet và các dạng cấu trúc khác
Cấu trúc bậc hai của protein diễn ra khi chuỗi polypeptide bắt đầu gấp cuộn thành các hình dạng cụ thể như α-helix và β-sheet. Đây là giai đoạn quan trọng trong việc tạo ra hình dạng và chức năng của protein.
α-helix
α-helix là một trong những cấu trúc phổ biến nhất trong protein. Nó được xác định bởi sự xoắn của chuỗi polypeptide quanh một trục trung tâm, với các liên kết hydro giữa các axit amin ở khoảng cách gần.
β-sheet
β-sheet là một kiểu cấu trúc khác trong protein, nơi các chuỗi polypeptide song song hoặc đối diện nhau và tạo thành một lớp gấp nếp. Các liên kết hydro giữa các chuỗi này giúp duy trì cấu trúc ổn định.
Những cấu trúc khác
Ngoài α-helix và β-sheet, còn có nhiều dạng cấu trúc khác như turn và loop, cũng đóng góp vào sự phong phú trong cấu trúc protein. Những cấu trúc này thường có vai trò trong việc tạo ra các vị trí hoạt động hoặc tương tác với các phân tử khác, làm tăng thêm khả năng linh hoạt cho protein.
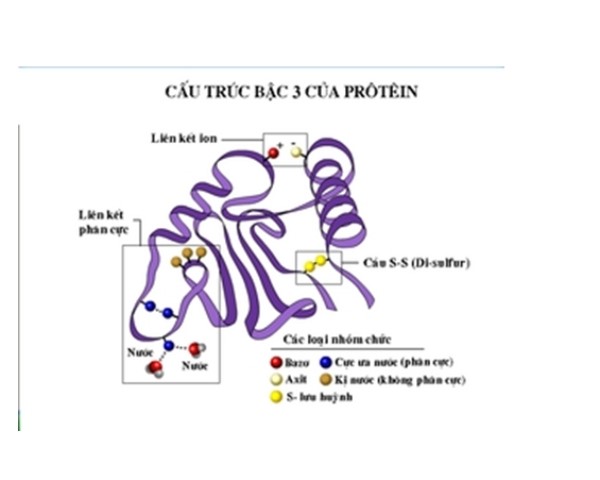
Cấu trúc bậc ba của Protein: Sự gấp cuộn không gian của chuỗi polypeptide
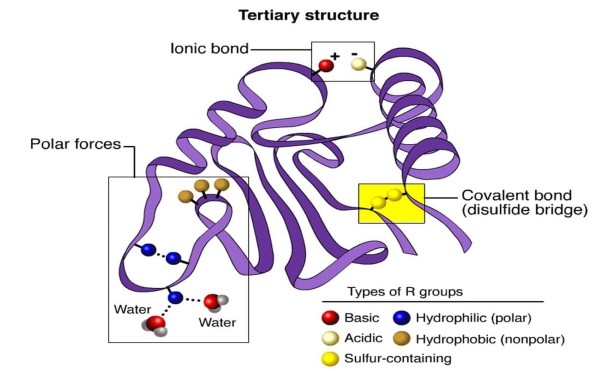
Cấu trúc bậc ba của protein là bước tiếp theo quan trọng sau bậc hai, nơi chuỗi polypeptide gấp cuộn thành hình dáng ba chiều phức tạp. Bậc cấu trúc này rất quan trọng vì nó ảnh hưởng trực tiếp đến chức năng của protein.
Các tương tác ổn định cấu trúc
Trong cấu trúc bậc ba, các tương tác giữa các chuỗi polypeptide như sự tương tác ion, liên kết hydro, và lực Van der Waals giúp ổn định hình dạng của protein. Ngoài ra, liên kết disulfide – một loại liên kết hóa học giữa cysteine – cũng đóng góp vào sự ổn định.
Tính linh hoạt của cấu trúc bậc ba
Cấu trúc bậc ba không phải là cố định; nó có thể thay đổi để phù hợp với các điều kiện khác nhau. Sự linh hoạt này rất quan trọng cho chức năng của enzym, cho phép chúng hoạt động một cách hiệu quả trong các phản ứng hóa học.
Ví dụ về cấu trúc bậc ba
Một ví dụ điển hình cho cấu trúc bậc ba là myoglobin – một loại protein vận chuyển oxy trong cơ. Hình dạng ba chiều của myoglobin cho phép nó dễ dàng liên kết với oxy, đảm bảo rằng cơ thể nhận đủ oxy cần thiết.
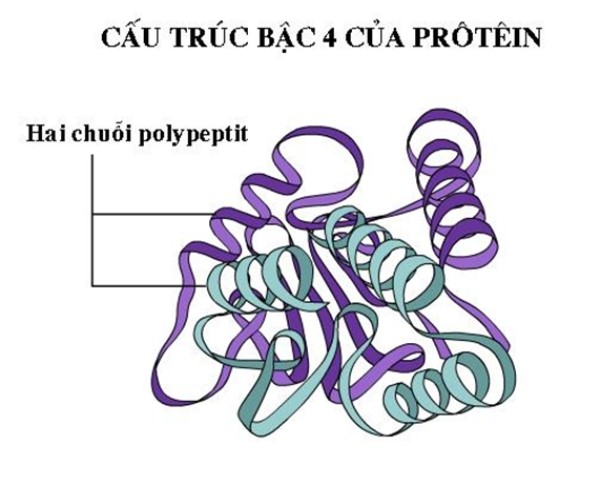
Cấu trúc bậc bốn của Protein: Sự tương tác giữa nhiều chuỗi polypeptide
Cấu trúc bậc bốn xuất hiện khi hai hoặc nhiều chuỗi polypeptide kết hợp với nhau để tạo thành một cấu trúc protein phức tạp hơn. Cấu trúc này là rất quan trọng cho chức năng của nhiều loại protein, đặc biệt là các enzym và hormone.
Tương tác giữa các chuỗi polypeptide
Sự tương tác giữa các chuỗi này có thể thông qua các liên kết yếu như liên kết hydro, liên kết ion, và lực Van der Waals. Cấu trúc bậc bốn không chỉ mang lại sự ổn định mà còn tạo ra các trung tâm hoạt động cần thiết cho chức năng của protein.
Ví dụ điển hình về cấu trúc bậc bốn
Hemoglobin là một ví dụ nổi bật cho cấu trúc bậc bốn. Nó được cấu thành từ bốn chuỗi polypeptide, giúp tạo ra một cấu trúc cho phép hemoglobin dễ dàng liên kết và vận chuyển oxy trong cơ thể.
Tính đa dạng của cấu trúc bậc bốn
Sự đa dạng trong cấu trúc bậc bốn cho phép protein hoạt động trong nhiều điều kiện khác nhau, từ môi trường axit đến kiềm. Điều này rất quan trọng trong các chức năng sinh lý của cơ thể, từ việc điều hòa hormone đến các phản ứng miễn dịch.
Vai trò của các liên kết yếu trong ổn định cấu trúc protein
Các liên kết yếu như liên kết hydro, lực Van der Waals và liên kết ion đóng vai trò thiết yếu trong việc ổn định cấu trúc của protein. Mặc dù các liên kết này không mạnh mẽ như liên kết hóa học, nhưng sự phối hợp hài hòa giữa chúng giúp protein giữ được hình dạng và chức năng.
Tác động của liên kết yếu
Liên kết yếu có tính linh hoạt cao, giúp cho protein có khả năng biến đổi hình dạng khi cần thiết. Điều này rất quan trọng trong các quá trình sinh lý như hoạt động của enzym, nơi mà hình dạng của protein phải thay đổi để tạo điều kiện cho phản ứng hóa học xảy ra.
Thay đổi cấu trúc do môi trường
Môi trường xung quanh có thể ảnh hưởng đến các liên kết yếu này. Ví dụ, sự thay đổi pH hay nồng độ muối có thể làm yếu đi các liên kết yếu, gây ra hiện tượng biến tính. Điều này có thể dẫn đến việc protein không còn hoạt động nữa, ảnh hưởng đến nhiều quá trình sinh học.
Nghiên cứu về liên kết yếu
Việc nghiên cứu các liên kết yếu không chỉ giúp chúng ta hiểu rõ hơn về cấu trúc protein mà còn có thể mở ra hướng đi mới cho việc phát triển thuốc và liệu pháp điều trị. Hiểu biết về cách mà các yếu tố môi trường tác động đến protein sẽ giúp tạo ra các sản phẩm sinh học an toàn và hiệu quả hơn.
Ảnh hưởng của các yếu tố môi trường đến cấu trúc protein
Các yếu tố môi trường như nhiệt độ, pH và nồng độ muối có ảnh hưởng đáng kể đến cấu trúc và chức năng của protein. Việc nghiên cứu những ảnh hưởng này rất quan trọng trong việc phát triển các ứng dụng công nghệ sinh học.
Độ pH
Độ pH của môi trường có thể ảnh hưởng đến sự ion hóa của các nhóm chức trong protein, từ đó làm thay đổi cấu trúc và chức năng của nó. Một số protein chỉ hoạt động tốt trong một khoảng pH nhất định, và nếu ra ngoài khoảng này, chúng có thể bị biến tính, mất khả năng hoạt động.
Nhiệt độ
Nhiệt độ cũng có vai trò quan trọng trong việc ổn định cấu trúc protein. Nhiệt độ cao có thể làm phá vỡ các liên kết yếu, dẫn đến biến tính protein. Ngược lại, nhiệt độ thấp có thể làm giảm tốc độ các phản ứng sinh hóa, ảnh hưởng đến khả năng hoạt động của protein.
Nồng độ muối
Nồng độ muối trong môi trường cũng ảnh hưởng đến cấu trúc protein. Muối có thể tạo ra các tương tác ion giữa các phân tử protein, từ đó ảnh hưởng đến hình dạng và chức năng của chúng. Việc điều chỉnh nồng độ muối có thể giúp duy trì ổn định cho protein, đặc biệt trong các ứng dụng sinh học.
Ứng dụng của kiến thức về cấu trúc protein trong y học và công nghệ sinh học
Kiến thức về cấu trúc protein không chỉ dừng lại ở lý thuyết mà còn có nhiều ứng dụng thực tiễn trong y học và công nghệ sinh học. Việc hiểu rõ cách thức hoạt động của protein có thể giúp phát triển các phương pháp điều trị hiệu quả hơn.

Phát triển thuốc
Hiểu biết về cấu trúc protein giúp các nhà nghiên cứu xác định được các mục tiêu thuốc tiềm năng. Điều này mở ra cơ hội cho việc phát triển các loại thuốc mới có tác dụng trực tiếp lên protein mục tiêu, từ đó cải thiện hiệu quả điều trị.
Thiết kế protein tái tổ hợp
Công nghệ sinh học hiện đại cho phép chúng ta thiết kế và sản xuất protein tái tổ hợp với chức năng cụ thể. Các protein này có thể được sử dụng trong liệu pháp gene, vaccine, và nhiều ứng dụng khác trong y học.
Nghiên cứu về bệnh lý
Nghiên cứu về cấu trúc protein cũng giúp chúng ta hiểu rõ hơn về cơ chế gây bệnh. Nhiều bệnh lý liên quan đến sự biến đổi cấu trúc protein, như Alzheimer và Parkinson. Việc tìm hiểu nguyên nhân và cơ chế này sẽ giúp phát triển các phương pháp điều trị hiệu quả hơn.
Các phương pháp nghiên cứu và xác định cấu trúc protein
Việc nghiên cứu và xác định cấu trúc protein là một lĩnh vực quan trọng trong sinh học phân tử. Có nhiều phương pháp khác nhau được sử dụng để nghiên cứu cấu trúc protein, từ kỹ thuật truyền thống đến các công nghệ tiên tiến.
Kỹ thuật tinh thể hóa
Tinh thể hóa protein là một trong những phương pháp phổ biến nhất để xác định cấu trúc. Khi protein được tinh thể hóa, các nhà nghiên cứu có thể sử dụng phương pháp tán xạ tia X để xác định vị trí và sắp xếp của các nguyên tử trong protein.
Kỹ thuật NMR
Kỹ thuật cộng hưởng từ hạt nhân (NMR) cũng được sử dụng để xác định cấu trúc protein. Phương pháp này cho phép theo dõi động lực học của protein trong môi trường gần giống như trong cơ thể, giúp hiểu rõ hơn về cách thức protein hoạt động.
Cryo-EM
Cryo-electron microscopy (Cryo-EM) là một công nghệ mới cho phép xem cấu trúc protein ở độ phân giải cực cao mà không cần tinh thể hóa. Đây là một bước tiến lớn trong nghiên cứu cấu trúc protein, giúp xác định hình dạng và tương tác của protein một cách nhanh chóng và chính xác.
Kết luận
Như vậy, protein có bao nhiêu bậc cấu trúc là một câu hỏi thú vị mở ra cánh cửa khám phá sâu rộng về thế giới sinh học. Qua việc tìm hiểu các bậc cấu trúc khác nhau của protein, từ bậc một đến bậc bốn, cùng với sự ảnh hưởng của các yếu tố môi trường và ứng dụng trong y học, chúng ta có thể thấy rằng cấu trúc protein không chỉ quan trọng trong nghiên cứu mà còn có giá trị thực tiễn trong cuộc sống. Kiến thức về protein không chỉ giúp chúng ta hiểu rõ hơn về cơ chế sự sống mà còn mở ra những cơ hội phát triển trong ngành y học và công nghệ sinh học trong tương lai.









